Мелфлуфен (мелфалан флуфенамид) је нови лек који се истражује у лечењу релапса или ватросталног мултиплог мијелома (РРММ). Дериват је лека за хемотерапију мелфалан. Мелфлуфен је коњугат пептид-лек; комбинација мелфалана и пептида (мали протеин) повезани заједно. Мелфлуфен се даје интравенском инфузијом (у вену).
Лек је поднет као нова пријава лека америчкој администрацији за храну и лекове (ФДА) у јулу 2020. ФДА је одобрила преглед приоритета пријаве и одлука се очекује крајем фебруара 2021. Мелфлуфен још увек није широко доступан јер није лиценциран и одобрен за употребу код мијелома. Међутим, пацијенти се могу лечити леком као део клиничког испитивања.
СимплеИмагес / Гетти Имагес
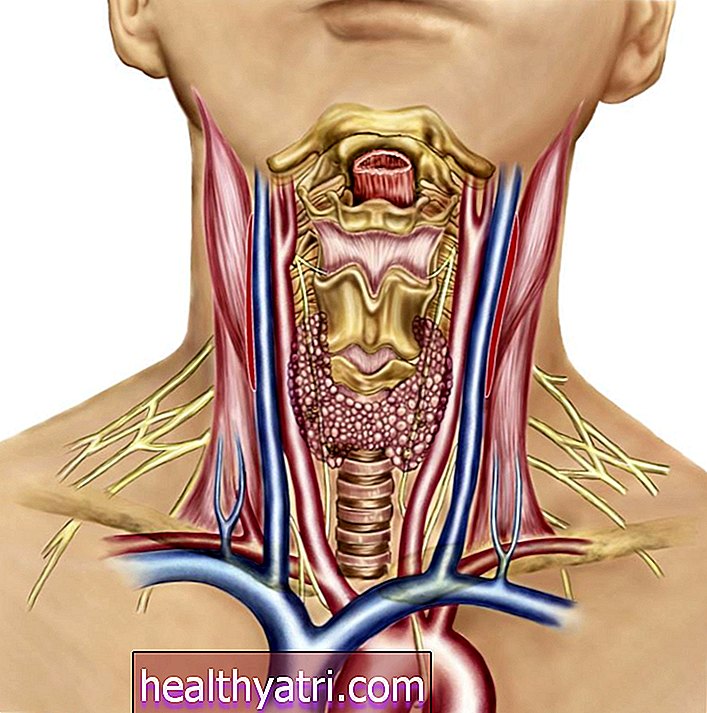
Шта је мултипли мијелом?
Вишеструки мијелом је врста ретког, неизлечивог карцинома крви, такође познатог као хематолошки рак. Утиче на ћелије зване плазма ћелије, које су врсте белих крвних зрнаца. Не постоји лек за мултипли мијелом и он се готово увек врати, а у том тренутку се каже да имате „рецидив или рефракторну“ болест.
Како Мелфлуфен делује?
Како се нове комбинације лекова против миелома уводе у раније линије терапије, људи са РРММ често имају болест отпорну на више лекова, па су хитно потребни лекови са новим механизмима деловања.
Мелфлуфен, у комбинацији са стероидом дексаметазоном, има потенцијал да испуни ову незадовољену медицинску потребу пружајући:
- Нов механизам деловања
- Клинички значајна ефикасност
- Управљива сигурност
Мелфлуфен убија ћелије мијелома употребом пептидаза (ензима који разграђују пептиде) који се често налазе у већем броју у ћелијама мијелома него у здравим ћелијама. Када мелфлуфен уђе у ћелије мијелома, пептидазе у ћелији прекидају везу која држи мелфалан и пептидаза заједно. Ово ослобађа активни мелфалан унутар ћелије мијелома. Мелфалан тада узрокује неповратно оштећење ДНК, што доводи до ћелијске смрти.
Шта истраживање каже
У току су истраживања како би се пронашли нови третмани мултиплог мијелома и развили начини за побољшање употребе постојећих.
Да бисте помогли у истраживању, од вас ће можда бити затражено да учествујете у клиничком испитивању током лечења.
Мелфлуфен се тренутно истражује као лек за пацијенте са РРММ-ом у условима клиничког испитивања. Клиничка испитивања која су испитивала ефикасност мелфлуфена укључују:
Студија О-12-М1
О-12-М1 је међународно мултицентрично испитивање фазе И / ИИ за утврђивање дозе мелфлуфена у комбинацији са дексаметазоном и испитивање одговора на лечење код пацијената са РРММ, који су били ватростални (отпорни) на последњу линију терапије. У
У студији О-12-М1, група од 45 пацијената који су примили најмање две претходне терапије уписани су између јула 2013. и децембра 2016. Суђење је настојало да открије максималну толерисану дозу мелфлуфена. Утврђена максимална толерисана доза била је 40 мг мелфлуфена у комбинацији са дексаметазоном.
Кохорта са највећом дозом (55 мг) премашила је максимално толерисану дозу, јер су четири од шест пацијената искусила озбиљне нежељене ефекте, укључујући неутропенију (низак ниво белих крвних зрнаца) и тромбоцитопенију (низак број тромбоцита); стога планирана највиша доза од 70 мг није тестирана.
За пробне пацијенте, лечење мелфлуфеном и дексаметазоном довело је до стабилизације болести код 76% пацијената.
Средње време до следећег лечења - почетка лечења до следећег лечења (или до смрти пацијента, шта год се десило пре) било је 7,9 месеци. Пацијенти су живели у просеку од 20,7 месеци.
Клиничко испитивање ХОРИЗОН
У фази ИИ клиничког испитивања ХОРИЗОН - које се одвијало на 20 локација широм Сједињених Држава и Европе - мелфлуфен и дексаметазон добили су укупно 154 пацијента који су у просеку примили пет претходних линија лечења.
Сви пацијенти су претходно лечени имуномодулаторним леком и инхибитором протеасома и били су резистентни на помалидомид и / или даратумумаб.
Отприлике три на сваких 10 пацијената (29%) одговорило је на лечење, а просечно време пре него што се мијелом почео враћати било је четири месеца. Ови резултати су показали да мелфлуфен може бити користан за пацијенте који су претходно имали више линија лечења.
Нежељени догађаји (АЕ) довели су до смањења дозе мелфлуфена код 27% пацијената и кашњења дозе код 61% пацијената. Најчешћа АЕ која је довела до смањења дозе била је тромбоцитопенија (низак број тромбоцита) која се појавила код 14% пацијената.
Озбиљна нежељена дејства су се појавила код 49% пацијената укупно; најчешће пријављене биле су упала плућа (9%) и неутропенија (5%). Други примарни малигнитети појавили су се код пет пацијената; од тога су четири имала малигне болести са кожним манифестацијама. Укупно је 10 пацијената (6%) умрло од нежељених ефеката повезаних са лечењем.
Дозирање
Мелфлуфен се даје интравенском инфузијом (у вену). У клиничким испитивањима, доза је била:
- 40 мг мелфлуфена првог дана сваког циклуса лечења
40 мг дексаметазона (смањена доза за пацијенте старије од 75 година) 1., 8., 15. и 22. дана сваког 28-дневног циклуса
У неким испитивањима доза је смањена код оних који су имали нежељене реакције.
Последице
Најчешће уочени нежељени ефекти мелфлуфена укључују:
• Низак број крвних зрнаца - неутропенија и тромбоцитопенија
• Анемија
• Умор
• Инфекције, укључујући упалу плућа и инфекције горњих дисајних путева
• Мучнина и дијареја
Будући да је мелфлуфен релативно нов лек, могу се појавити нови нежељени ефекти који још увек нису пријављени.
Ризици
Како су истраживања у току, тешко је проценити ризике узимања мелфлуфена за РРММ. Како су пацијенти регрутовани за клиничка испитивања често исцрпљивали претходне третмане, шансе за нежељене ефекте или чак смрт током и после лечења су могуће.
Инфекције су главни узрок морбидитета и морталитета код пацијената са РРММ, услед исцрпљеног имунолошког система. Важно је да се редовно надгледате због знакова инфекције и да што пре пријавите лекару.