Вирус хумане имунодефицијенције (ХИВ) је ретровирус чији су гени кодирани рибонуклеинском киселином (РНК) уместо деоксирибонуклеинске киселине (ДНК).
Ретровирус се разликује од традиционалног вируса по начину на који заражава, реплицира и узрокује болест.
ХИВ је један од само два људска ретровируса своје класе, од којих је други хумани Т-лимфотропни вирус (ХТЛВ).
Тхана Прасонгсин / Гетти Имагес
Шта је ретровирус?
ХИВ и ХТЛВ су класификовани као породични РНК вируси ИВ групеРетровиридае.Они раде тако што убацују свој генетски материјал у ћелију, а затим мењају њену генетску структуру и функцију како би се реплицирали.
ХИВ је даље класификован као лентивирус, врста ретровируса који се везује за специфични протеин назван ЦД4.
Ретровиридаевируси могузаразе сисаре (укључујући људе) и птице и познати су по томе што изазивају поремећаје имунодефицијенције, као и туморе.
Њихова карактеристика која дефинише је ензим назван реверзна транскриптаза, који транскрибује РНК у ДНК.
У већини случајева, ћелије претварају ДНК у РНК како би се могле направити од различитих протеина. Али код ретровируса, овај процес се дешава обрнуто (дакле „ретро“ део), где се вирусна РНК претвара у ДНК.
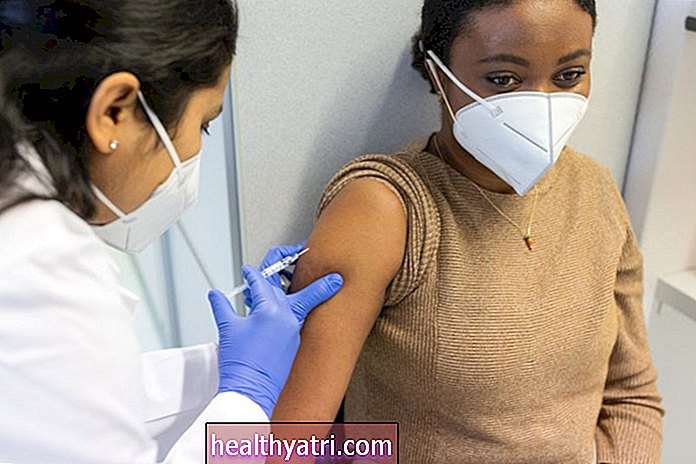
Како ХИВ зарази
ХИВ се разликује од ХТЛВ-а по томе што је последњи делтаретровирус. Иако се за обе карактерише обрнута транскрипција, лентивируси се агресивно реплицирају, док делтаретровируси имају минималну активну репликацију када се утврди инфекција.
Да би ХИВ могао да зарази друге ћелије у телу, он пролази кроз животни циклус (или репликацију) у седам корака, што резултира претварањем ћелије домаћина у фабрику која ствара ХИВ. Ево шта се дешава:
- Везивање: Након проналаска и напада ЦД4 ћелије, ХИВ се везује за молекуле на површини ЦД4 ћелије.
- Фузија: Једном када су ћелије повезане, вирусна коверта ХИВ-а се стапа са ћелијском мембраном ЦД4, омогућавајући ХИВ-у да уђе у ЦД4 ћелију.
- Обрнута транскрипција: Након што се нађе унутар ЦД4 ћелије, ХИВ ослобађа, а затим користи ензим реверзне транскриптазе да претвори своју РНК у ДНК.
- Интеграција: Обрнута транскрипција даје ХИВ прилику да уђе у језгро ЦД4 ћелије, када једном уђе у њу, ослобађа други ензим зван интеграза, који користи за уметање своје вирусне ДНК у ДНК ћелије домаћина.
- Репликација: Сада када је ХИВ интегрисан у ДНК ћелије домаћина домаћина, почиње да користи машине које се већ налазе у ћелији ЦД4 за стварање дугих ланаца протеина, који су градивни блокови за више ХИВ-а.
- Скуп: Сада се нова ХИВ РНА и ХИВ протеини произведени од ЦД4 ћелије домаћина премештају на површину ћелије и формирају незрели (неинфективни) ХИВ.
- Пупање: Овај незрели ХИВ - који није у стању да зарази другу ЦД4 ћелију - затим на силу излази из ЦД4 ћелије домаћина. Тамо ослобађа још један ХИВ ензим зван протеаза, који прекида дуге протеинске ланце у незрелом вирусу. Притом ствара зрели - и сада заразни - вирус, који је сада спреман да зарази друге ЦД4 ћелије.
Циљеви за терапију
Разумевањем горе описаних механизама репликације, научници су у стању да циљају и блокирају одређене фазе животног циклуса ХИВ-а.
Прекидајући његову способност репликације, популација вируса може бити сузбијена до нивоа који се не може утврдити, што је и циљ ХИВ антиретровирусних лекова.
Тренутно постоји девет различитих класа антиретровирусних лекова који се користе за лечење ХИВ-а, груписаних према стадијуму животног циклуса који блокирају:
Инхибитор уноса / прилога
Шта раде: Вежу се за протеин на спољној површини ХИВ-а, спречавајући ХИВ да уђе у ЦД4 ћелије.
Лек (и) у овој класи: Фостемсавир
Инхибитор након везивања
Шта раде: Блокирају ЦД4 рецепторе на површини одређених имуних ћелија које ХИВ треба да уђе у ћелије.
Лек (и) у овој класи: Ибализумаб-уиик
Инхибитор фузије
Шта раде: Блокирају ХИВ да уђе у ЦД4 ћелије имуног система.
Лек (и) у овој класи: Енфувиртиде
ЦЦР5 Антагонисти
Шта раде: Блокирају ЦЦР5 корецепторе на површини одређених имуних ћелија којима ХИВ треба да уђе у ћелије.
Лек (и) у овој класи: Маравироц
Нуклеозидни инхибитори реверзне транскриптазе (НРТИ)
Шта раде: Блокирају реверзну транскриптазу, ензим ХИВ треба да направи своје копије.
Лекови у овој класи: Абакавир, емтрицитабин, ламивудин, тенофовирдизопроксил фумарат, зидовудин
Ненуклеозидни инхибитори реверзне транскриптазе (ННРТИ)
Шта раде: Везују се и касније мењају реверзну транскриптазу, ензим ХИВ треба да направи своје копије.
Лекови у овој класи: Доравирин, ефавиренз, етравирин, невирапин, рилпивирин
Инхибитори протеазе (ПИ)
Шта раде: Блокирају ХИВ протеазу, ензим ХИВ треба да направи своје копије.
Лекови у овој класи: Атазанавир, дарунавир, фосампренавир, ритонавир, саквинавир, типранавир
Инхибитор преноса ланца интеграсе (ИНСТИ)
Шта раде: Блокирају ХИВ интегразу, ензим ХИВ треба да направи своје копије.
Лекови у овој класи: каботегравир, долутегравир, ралтегравир
Побољшавачи фармакокинетике ("појачивачи")
Шта раде: Користе се у лечењу ХИВ-а за повећање ефикасности лекова за ХИВ укључених у режим ХИВ-а.
Лек (и) у овој класи: Цобицистат
Зашто не постоји један антиретровирусни лек који може све?
Због велике генетске варијабилности ХИВ-а, комбинована антиретровирусна терапија је потребна да би се блокирале различите фазе животног циклуса и обезбедила трајна супресија. До данас ниједан антиретровирусни лек није у стању да то уради.
Изазови и циљеви
Лентивируси се агресивно реплицирају - са временом удвостручавања од 0,65 дана током акутне инфекције - али тај процес репликације је склон грешкама. То се преводи у високу стопу мутације, током које се у току дана може развити вишеструке варијанте ХИВ-а код особе.
Многе од ових варијанти су неживотне и не могу преживети. Други су одрживи и представљају изазове за лечење и развој вакцина.
Отпорност на лекове
Један од значајних изазова за ефикасно лечење ХИВ-а је способност вируса да мутира и репродукује се док особа узима антиретровирусне лекове.
Ово се назива ХИВ резистенција на лекове (ХИВДР) и може угрозити ефикасност тренутних терапијских опција и циљ смањења ХИВ инциденце, морталитета и морбидитета.
ХИВ дивљег типа
Отпорност на лекове за ХИВ може се развити као резултат нечега познатог као „дивљи тип“ ХИВ-а, који је претежна варијанта у нелеченом вирусном базену, захваљујући чињеници да може преживети када друге варијанте не могу.
Вирусна популација може почети да се мења само када особа почне да узима антиретровирусне лекове.
Будући да се нелечени ХИВ тако брзо реплицира и често укључује мутације, могуће је да се створи мутација која може да зарази ћелије домаћина и преживи - чак и ако особа узима антиретровирусне лекове.
Такође је могуће да мутација отпорна на лекове постане доминантна варијанта и размножава се. Поред тога, резистенција се може развити као резултат лошег придржавања лечења, што доводи до вишеструке резистенције на лекове и неуспеха лечења.
Понекад, када су људи ново заражени ХИВ-ом, наслеђују резистентни сој вируса од особе која их је заразила - нешто што се назива пренесена резистенција. Чак је могуће да неко новоинфицирани наследи дубоку резистенцију на више лекова против неколико класа лекова против ХИВ-а.
Новији третмани против ХИВ-а нуде већу заштиту од мутација
Тамо где неки старији ХИВ лекови попут Вирамуне (невирапин) и Сустива (ефавиренз) могу развити ХИВ резистенцију са само једном мутацијом, новији лекови захтевају бројне мутације пре него што се догоди неуспех.
Развој вакцина
Једна од најзначајнијих препрека стварању широко ефикасне вакцине против ХИВ-а је генетска разноликост и варијабилност самог вируса. Уместо да се могу фокусирати на један сој ХИВ-а, истраживачи морају да узму у обзир чињеницу да се он тако брзо реплицира.
Циклус репликације ХИВ-а
Циклус репликације ХИВ-а траје нешто више од 24 сата.
И док је поступак репликације брз, није најтачнији - сваки пут се ствара много мутираних копија, које се затим комбинују и формирају нове сојеве док се вирус преноси између различитих људи.
На пример, у ХИВ-1 (један сој ХИВ-а) постоји 13 различитих подтипова и подтипова који су географски повезани, са 15% до 20% варијација унутар подтипова и до 35% између подтипова.
Ово није само изазов у стварању вакцине, већ и зато што су неки мутирани сојеви отпорни на АРТ, што значи да неки људи имају агресивнију мутацију вируса.
Још један изазов у развоју вакцине је нешто што се назива латентни резервоари, а који се успостављају у најранијој фази ХИВ инфекције и могу ефикасно „сакрити“ вирус од имунолошког откривања, као и од ефеката АРТ-а.
То значи да ако се икада заустави лечење, латентно заражена ћелија може се реактивирати, што доводи до тога да ћелија поново почне да производи ХИВ.
Иако АРТ може сузбити ниво ХИВ-а, не може елиминисати латентне резервоаре ХИВ-а, што значи да АРТ не може излечити ХИВ инфекцију.
Изазови латентних резервоара за ХИВ
Док научници не успеју да „очисте“ латентне резервоаре за ХИВ, мало је вероватно да ће било која вакцина или терапијски приступ у потпуности искоријенити вирус.
Ту је и изазов имунолошке исцрпљености која долази са дуготрајном ХИВ инфекцијом. Ово је постепени губитак способности имунолошког система да препозна вирус и покрене одговарајући одговор.
Било која врста ХИВ вакцине, лека против АИДС-а или другог третмана мора се створити узимајући у обзир исцрпљеност имунитета, проналажење начина за решавање и умањивање опадајућих способности имунолошког система особе током времена.
Напредак у истраживању вакцина против ХИВ-а
Међутим, постигнут је одређени напредак у истраживању вакцина, укључујући експерименталну стратегију названу „шутни и убиј“. Надамо се да комбинација агенса за смањење кашњења са вакцином (или другим средствима за стерилизацију) може успети лековитом, експерименталном стратегијом познатом под називом „шутни и убиј“ (или „шок и убиј“).
У основи, то је процес у два корака:
- Прво, лекови који се зову агенси за уклањање латенције користе се за реактивацију латентног ХИВ-а који се скрива у имунолошким ћелијама (део „ударца“ или „шока“).
- Тада, након што се имуне ћелије поново активирају, имунолошки систем тела - или лекови против ХИВ-а - могу да циљају и убију реактивиране ћелије.
Нажалост, само агенси за реверзирање латенције нису способни да смање величину вирусних резервоара.
Поред тога, неки од најперспективнијих модела вакцина до данас укључују широко неутрализујућа антитела (бНАбс) - ретку врсту антитела која је у стању да циља већину варијанти ХИВ-а.
БНАбс су први пут откривени у неколико ХИВ елитних контролора - људи који изгледа имају способност сузбијања репликације вируса без АРТ-а и не показују доказе о напредовању болести. Нека од ових специјализованих антитела, попут ВРЦ01, способна су да неутралишу више од 95% варијанти ХИВ-а.
Тренутно истраживачи вакцина покушавају да стимулишу производњу бНАб.
Студија из 2019. која укључује мајмуне показује обећања. Након што су примили једну ињекцију вакцине против ХИВ-а, шест од 12 мајмуна у испитивању развило је антитела која су значајно одложила инфекцију, а - у два случаја - чак и спречила.
Овај приступ је још увек у раној фази испитивања на људима, иако је у марту 2020. објављено да су научници први пут успели да осмисле вакцину која је индуковала људске ћелије да генеришу бНАб.
Ово је значајан развој, након година прошлих студија, које су до овог тренутка биле ометене недостатком снажног или специфичног одговора на бНАб.
ХИВ вектори у генској терапији
Инактивирани ХИВ се сада истражује као потенцијални систем испоруке за лечење других болести - укључујући:
- Леукемија
- Тешка комбинована имунодефицијенција (СЦИД)
- Метакроматска леукодистрофија
Претварајући ХИВ у неинфективни „вектор“, научници верују да могу да користе вирус за испоруку генетског кодирања ћелијама које ХИВ првенствено зарази.
Реч од врло доброг
Бољим разумевањем начина на који ретровируси делују, научници су успели да развију нове лекове.
Али иако сада постоје могућности лечења које раније нису постојале, најбоље шансе особе да живи дуг, здрав живот са ХИВ-ом своди се на то да јој се дијагностикује што је раније могуће, редовним тестирањем.
Рана дијагноза значи ранији приступ лечењу - а да не спомињемо смањење болести повезане са ХИВ-ом и повећање очекиваног животног века.
-and-hiv.jpg)