Упркос више од 35 година истраживања, научници још увек нису пронашли лек за вирус хумане имунодефицијенције (ХИВ): вирус који узрокује синдром стечене имунодефицијенције (АИДС).
Антиретровирусна терапија (АРТ) била је велики пробој који помаже у сузбијању вируса, али није лек. И док је било неколико добро објављених случајева у којима се говорило да је ХИВ излечен - укључујући и случај Тимотхија Бровна, званог берлински пацијент - још увек није постојао приступ који може доследно и безбедно искоријенити ХИВ на индивидуалној основи , а још мање на глобалном нивоу. Упркос томе, напредује се.
ТЕК СЛИКА / ЗНАНСТВЕНА ФОТОГРАФИЈА / Гетти Имагес
Изазови
Постоји неколико разлога зашто је проналазак лека за ХИВ / АИДС био тако дуг пут изазова за изазовима. ХИВ је толико сложен, вишезначан вирус који се непрестано мења и отежава његово праћење.
Неки од тренутних општих изазова са којима се суочавају ХИВ истраживања укључују:
- Досезање популација које су у највећем ризику од заразе и преноса ХИВ-а
- Осигуравање да се истраживање одвија уз потпуно информисани пристанак учесника, што значи да они у потпуности разумеју и ризике и користи суђења
- Развој сигурних и ефикасних кандидата за вакцину против ХИВ-а за тестирање кроз клиничка испитивања са приматима и са људима и са људима
- Боље разумевање механизама имуног одговора код људи
- Узимајући у обзир попратне болести ХИВ-а у истраживању, тако да би сваки потенцијални лек извукао корист што већем броју људи
- Све већи фокус на проучавању ремисије примећен код ретких пацијената који су прекинули лечење
- Дефинисање тачно шта се подразумева под „леком“ за ХИВ
- Смањивање стигме која још увек окружује ХИВ, са циљем да се минимализује његов утицај на учешће у истраживањима ХИВ-а
- Стицање бољег разумевања како ефикасно лечити ХИВ инфекције и управљати неуспехом у лечењу
Смањење преноса
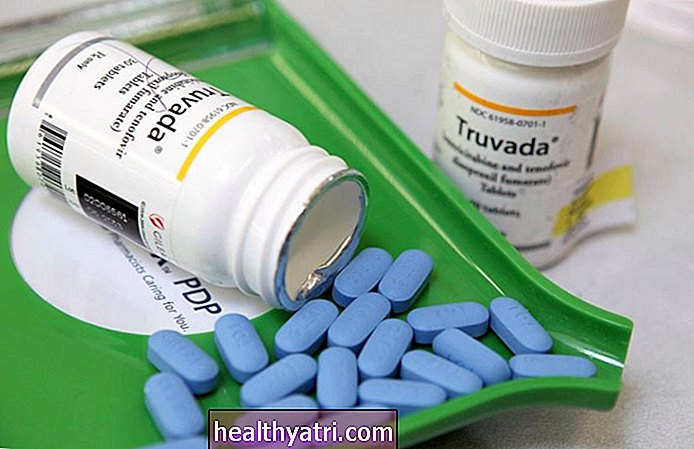
Иако то само по себи није „лек“, стратегија „лечења као превенција“ (ТасП) - која укључује свакодневно узимање лекова за ХИВ - била је врло ефикасна у смањењу преноса за оне који су већ ХИВ позитивни.
Штавише, 2020. године објављено је да је животни век особа са ХИВ-ом у Сједињеним Државама иста као и оних који никада нису били заражени вирусом - иако су уживали много мање година доброг здравља.
Идеално би било да следећи корак буде развој сигурне и ефикасне вакцине против ХИВ-а, али тренутно постоје неки изазови на путу напретку који је постигнут истраживањем.
Генетска променљивост
Једна од најзначајнијих препрека стварању широко ефикасне вакцине против ХИВ-а је генетска разноликост и варијабилност самог вируса.
Изазов циклуса репликације
Уместо да могу да се усредсреде на један сој ХИВ-а, истраживачи морају узети у обзир чињеницу да се он тако брзо реплицира, што може проузроковати мутације и нове сојеве. Циклус репликације ХИВ-а траје нешто више од 24 сата.
И док је поступак репликације брз, није најтачнији - сваки пут се ствара много мутираних копија, које се затим комбинују и формирају нове сојеве док се вирус преноси између различитих људи.
На пример, у ХИВ-1 (један сој ХИВ-а) постоји 13 различитих подтипова и подтипова који су географски повезани, са 15% до 20% варијација унутар подтипова и варијација до 35% између подтипова.
Ово није само изазов у стварању вакцине, већ и зато што су неки мутирани сојеви отпорни на АРТ, што значи да неки људи имају агресивнију мутацију вируса.
Латентни резервоари
Поред стално развијајућих и мутирајућих сојева ХИВ-а, још један изазов у развоју вакцине је нешто што се назива латентни резервоари. Они се успостављају током најраније фазе ХИВ инфекције и могу ефикасно „сакрити“ вирус од имунолошког откривања, као и од ефеката АРТ-а.
То значи да ако се икада заустави лечење, латентно заражена ћелија може се реактивирати, што ће довести до тога да ћелија поново почне да производи ХИВ.
Иако АРТ може сузбити ниво ХИВ-а, не може елиминисати латентне резервоаре ХИВ-а, што значи да АРТ не може излечити ХИВ инфекцију.
Исцрпљеност имунитета
Ту је и изазов имунолошке исцрпљености која долази са дуготрајном ХИВ инфекцијом. Ово је постепени губитак способности имунолошког система да препозна вирус и покрене одговарајући одговор.
Свака врста ХИВ вакцине, лека против АИДС-а или другог третмана мора се створити узимајући у обзир исцрпљеност имунитета, проналажење начина за решавање и ублажавање опадајућих способности имунолошког система особе током времена.
Рани напредак
Иако је напредак постигнут у излечењу ХИВ-а спор, на путу је још увек било трачака наде, што указује на то да се научници можда приближавају широко ефикасном лечењу.
Берлински пацијент
Можда најпознатији случај до сада био је Тимоти Браун, познат и као „берлински пацијент“, који се сматра првом особом која је „функционално излечена“ од ХИВ-а.
Упркос свом надимку, Бровн је рођен у Сједињеним Државама, али му је ХИВ дијагностикован 1995. године током студија у Немачкој. Десет година касније, дијагностикована му је акутна мијелоична леукемија (АМЛ) и била му је потребна трансплантација матичних ћелија како би имао било какве шансе да преживи рак.
Када су лекари открили да се Бровн подудара са 267 давалаца (многи људи не пронађу ниједну подударност), одлучили су да користе ону која је имала мутацију названу ЦЦР5-делта 32, за коју се сматра да може да индукује ХИВ имунитет.
Три месеца након његове трансплантације у фебруару 2007. године, ХИВ више није откривен у Брауновој крви. И док је и даље имао компликације са леукемијом - и била му је потребна додатна трансплантација матичних ћелија - Браунова ХИВ инфекција се није вратила. То је остало до његове смрти 2020. године од леукемије.
Лекари из Бригхам-а и Женске болнице у Бостону покушали су да користе сличну технику трансплантације матичних ћелија код два пацијента између 2008. и 2012. године - мада без употребе давалаца са мутацијом делта 32. Иако су пацијенти у почетку имали 10 и 13 месеци неоткривених нивоа ХИВ-а, обојица су потом прошли кроз вирусни поврат.
Лондонски пацијент
Објављена је студија из 2019. године која је пружила детаље у вези са другом особом - Адамом Цастиллејо, овог пута познатим као „Лондонски пацијент“ - који је такође изгледа функционално излечен од ХИВ-а.
Његова ситуација била је слична оној са Брауновом јер је имао рак, примио је хемотерапију да би уништио свој имуни систем, а затим је имао трансплантацију матичних ћелија користећи донорске ћелије са генетском мутацијом која доводи до ХИВ имунитета.
До сада постоје клинички докази да је Цастиллејо 30 месеци био у ремисији ХИВ-1 без вируса компетентног за репликацију, мада је нејасно да ли ће се наставити.
И иако је употреба трансплантације матичних ћелија за производњу имунитета на ХИВ можда била успешна за Бровн и Цастиллејо, то није нешто што ће се ускоро користити у редовном клиничкој пракси у свом садашњем облику.
Овај поступак у више корака не само да је скуп, већ укључује и превише потенцијалних ризика и штете за пацијента.
Будући да су и Бровн и Цастиллејо оболели од рака и ионако им је била потребна трансплантација матичних ћелија, проналажење даваоца са мутацијом делта 32 имало је смисла. Међутим, није одржива опција да се неко без рака подвргне овом специфичном курсу лечења.
Упркос практичним ограничењима лечења, ови случајеви су научницима пружили увид у напредна истраживања излечења од ХИВ-а на значајне начине.
Генска терапија заснована на матичним ћелијама
Једна врста лечења која показује почетни потенцијал је генска терапија заснована на матичним ћелијама - приступ који је у великој мери утемељен на Бровновом случају.
Његов циљ је да реконституише особу са имунолошким системом ХИВ-а трансплантацијом генетски модификованих крвотворних матичних ћелија са анти-ХИВ генима, који се не само могу обновити, већ се могу и умножавати и диференцирати у зреле имуне ћелије.
Постигнут је одређени успех у раним истраживањима генске терапије засноване на матичним ћелијама.
Студија из 2018. године која укључује ХИВ-заражене мајмуне макака пигтаила открила је да је трансплантација генетски уређених матичних ћелија успела да значајно смањи величину њихових успаваних „вирусних резервоара“ који би се могли поново активирати да би произвели додатне копије вируса.
Од тада је постигнут додатни напредак код примата. Према студији из 2021. године, истраживачи су утврдили формулу која би предвидела идеалну дозу матичних ћелија потребну за лечење ХИВ-а.
Још увек треба обавити посао
Иако је приступ показао обећање код примата, он се никако не може поновити на глобалном нивоу.
Сада је циљ поновити ефекте трансплантације матичних ћелија Брауна и Цастиллеја код других људи, али без токсичности да се прво мора подвргнути хемотерапији.
Широко неутралишућа антитела
Неки од најперспективнијих модела вакцина до данас укључују широко неутралишућа антитела (бНАбс) - ретку врсту антитела која је у стању да циља већину варијанти ХИВ-а.
БНАбс су први пут откривени у неколико ХИВ елитних контролора - људи који изгледа имају способност сузбијања репликације вируса без АРТ-а и не показују доказе о напредовању болести. Нека од ових специјализованих антитела, попут ВРЦ01, способна су да неутралишу више од 95% варијанти ХИВ-а.
Тренутно истраживачи вакцина покушавају да стимулишу производњу бНАб.
Студија из 2019. која укључује мајмуне показује обећања. Након што су примили једну ињекцију вакцине против ХИВ-а, шест од 12 мајмуна у испитивању развило је антитела која су значајно одложила инфекцију, а у два случаја су је чак и спречила.
бНАбс показују обећање
Овај приступ је још увек у раној фази испитивања на људима, иако је у марту 2020. објављено да су научници први пут успели да осмисле вакцину која је индуковала људске ћелије да генеришу бНАб.
Ово је значајан развој, након година прошлих студија, које су до овог тренутка биле ометене недостатком снажног или специфичног одговора на бНАб.
Преокрет кашњења
Док научници не успеју да „очисте“ латентне резервоаре за ХИВ, мало је вероватно да ће било која вакцина или терапијски приступ у потпуности искоријенити вирус.
Неки агенси, укључујући инхибиторе ХДАЦ који се користе у терапији рака, обећавају, али још увек нису успели да постигну висок ниво клиренса без ризика од токсичности. Поврх свега, научници остају несигурни колико су заправо ти резервоари опсежни.
Ипак, надамо се да комбинација агенса за уклањање кашњења са вакцином (или другим средствима за стерилизацију) може успети лековитом, експерименталном стратегијом познатом под називом „шутни и убиј“ (ака „шок и убиј“) који је тренутно под истрагом.
Кицк-анд-Килл стратегија
То је процес у два корака:
- Прво, лекови који се зову агенси за уклањање латенције користе се за реактивацију латентног ХИВ-а који се скрива у имунолошким ћелијама (део „ударца“ или „шока“).
- Тада, након што се имуне ћелије поново активирају, имунолошки систем тела - или лекови против ХИВ-а - могу да циљају и убију реактивиране ћелије.
Нажалост, само агенси за реверзирање латенције нису способни да смање величину вирусних резервоара.
Друга стратегија преокрета латенције може укључивати ПД-1 инхибиторе попут Кеитруде (пембролизумаб) који су показали обећања у чишћењу вирусних резервоара, док потенцијално укидају исцрпљеност имунитета.
ПД-1 делује као имунолошки контролни пункт и преференцијално се изражава на површини упорно заражених ћелија. Али у овом тренутку још увек није јасно да ли ПД-1 игра функционалну улогу у кашњењу ХИВ-а и истрајности резервоара.
Реч од врло доброг
Иако се напредује ка постизању лека за ХИВ, прерано је рећи када би могло доћи до открића.
Срећом, научници су постигли велики напредак у превенцији ХИВ-а - нарочито кроз профилаксу пре излагања (или ПрЕП). Идеја која стоји иза ПрЕП-а је да се људима са великим ризиком да заразе ХИВ-ом, али нису заражени, пружи могућност да се спречи тако што ће се узимати таблете једном дневно. Када се правилно и доследно користи, ПрЕП смањује ризик од ХИВ-а сексом за око 99%, а од ињектирања дроге за 74%.
Али док се не нађе лек, најбољи исход за људе са ХИВ-ом је антиретровирусна терапија, која може смањити ризик од болести повезаних са ХИВ-ом и задржати очекивани животни век - за оне у Сједињеним Државама - на сличној дужини као и они који немају имају ХИВ.