
Сасиистоцк / Гетти Имагес
Кључне Такеаваис
- Пфизер је добио одобрење ФДА да започне тестирање своје вакцине против коронавируса код деце 12 и више година.
- Стручњаци кажу да је укључивање деце у клиничка испитивања пресудно за укупан развој вакцине која ће заштитити и децу и одрасле од ЦОВИД-19.
- Према својој веб страници, Пфизер је у своју студију већ уписао више од 39.000 добровољаца. Више од 34.000 тих добровољаца већ је примило другу вакцинацију.
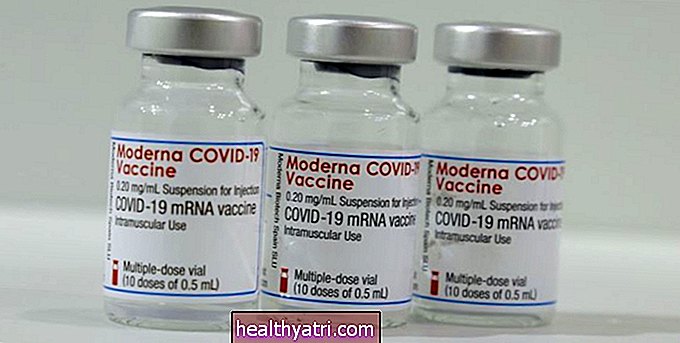
Америчка фармацеутска компанија Пфизер саопштила је у октобру да је добила дозволу америчке Управе за храну и лекове (ФДА) да започне упис деце од 12 година у своја испитивања вакцине против коронавируса.
„Чинећи то, моћи ћемо боље да разумемо потенцијалну сигурност и ефикасност вакцине код појединаца из више узраста и порекла“, рекла је компанија у ажурираној изјави.
Ово ће бити прво испитивање вакцине против ЦОВИД-19 у САД које је обухватило децу. Од октобра, Пфизер је једна од четири америчке компаније које имају вакцине у 3. фази клиничких испитивања.
Пфизер је већ проширио фазу 3 испитивања на децу од 16 и више година, као и људе са хроничним, стабилним вирусом хумане имунодефицијенције (ХИВ), хепатитисом Ц и хепатитисом Б.
Зашто тестирати ЦОВИД-19 вакцину на деци?
Пре него што је Пфизер стекао одобрење за започињање тестирања на деци, стручњаци су објавили извештај у часописуКлиничке заразне болестинаводећи значај таквог испитивања.
„Директни утицај ЦОВИД-19 на децу већи је од оног који је примећен код бројних других патогена за које сада имамо ефикасне педијатријске вакцине“, напомиње се у извештају. „Поред тога, улога деце у преношењу САРС-ЦоВ-2 је очигледно подцењена. Пажљиво спроведена клиничка испитивања фазе 2 могу на адекватан начин да реше потенцијалне проблеме са сигурношћу вакцине против ЦОВИД-19. “
Сузанне Пхам, доктор медицине
Не можемо превазићи ширење овог вируса ако не вакцинишемо своју децу.
- др Сузанне ПхамСхарон Нацхман, др. Мед., Шеф Одељења за дечије инфективне болести у Дечјој болници Стони Броок у Њујорку, слаже се са извештајем, говорећи Веривелл-у да су „педијатри веома заинтересовани да виде детаље студије и како ће вакцина деловати код деце. . “
Према Нацхман-у, специфичне користи имају тестирање вакцине код деце. Истраживачи ће моћи да процене краткорочни и дугорочни имунолошки одговор, што укључује утврђивање да ли је доза вакцине која се користи код одраслих неопходна деци или би они имали сличан имунолошки одговор као нижа доза.
Нацхман каже да је такође важно напоменути да, будући да коронавирусу код одраслих може претходити њихова изложеност асимптоматској инфекцији код деце, успостављање вакцине за лечење целе породице могло би „много да смањи преношење вируса код куће и у заједници“.
Сузанне Пхам, др.мед., Сарадник главног медицинског службеника у Меморијалној болници Веисс у Чикагу, каже Веривелл-у да што пре деца могу да се вакцинишу, пре ће се смањити стопе преноса.
„Ефикасним вакцинисањем деце смањит ће се ризик да дјеца преносе вирус унутар заједнице, посебно оним високоризичним људима који су подложнији тешким или критичним болестима“, каже Пхам за Веривелл. „Ово ће омогућити школама да се поново отворе и да се активности од виталног значаја за развој наше деце наставе на контролисан начин. Не можемо превазићи ширење овог вируса ако не вакцинишемо своју децу. Морамо имати довољно имунитета стада у друштву да бисмо могли спречити ширење “.
ЦОВИД-19 вакцине: Будите у току са доступним вакцинама, ко их може добити и колико су сигурне.
Како започињу испитивања вакцина?
Пхам објашњава да да би се вакцина тестирала - на одраслима или деци - компанија мора прво да поднесе ФДА пријаву за истражни нови лек (ИНД).
Апликација ће описати вакцину, како се производи и који тестови контроле квалитета ће се користити. Апликација такође укључује податке из испитивања на животињама који показују да је вакцина сигурна за почетно тестирање на људима.
Као што објашњава ФДА, поступак пријаве има неколико корака:
Током раног предклиничког развоја новог лека, главни циљ спонзора је да утврди да ли је производ разумно безбедан за почетну употребу код људи и да ли једињење показује фармаколошку активност која оправдава комерцијални развој.
Када се производ препозна као одржив кандидат за даљи развој, спонзор се затим фокусира на прикупљање података и информација потребних да би се утврдило да производ неће излагати људе неразумним ризицима када се користи у ограниченим клиничким студијама у раној фази.
Затим ће вакцина бити подвргнута испитивањима фазе 1, за које Пхам објашњава да су „студије сигурности и имуногености урађене на малом броју људи који су пажљиво праћени“.
„Фаза 2 се састоји од студија о распону доза и проширена је на већи број (стотине) људи“, каже Пхам. „Тада суђења у фази 3 настоје да упишу хиљаде људи како би документовали ефикасност и наставили да истражују безбедносне податке.“
Према својој веб страници, Пфизер је у своју студију уписао више од 39.000 добровољаца. Више од 34.000 њих примило је другу дозу вакцине.
Шта ово значи за вас
Клиничко испитивање фазе 3 које укључује испитивање ЦОВИД-19 вакцине код деце знак је напретка. Међутим, вакцина не може да се пожури. За довршавање резултата потребно је време да се заштити безбедност учесника испитивања, као и одраслих и деце која ће на крају добити готову верзију вакцине.

















-for-kids-with-autism.jpg)



