
Гетти Имагес
Кључне Такеаваис
- Управа за храну и лекове (ФДА) захтеваће од произвођача вакцина да обезбеде два месеца података о безбедности пре него што одобри ЦОВИД-19 вакцину за употребу у широј јавности.
- ФДА верује да ће двомјесечни период омогућити довољно времена да се појаве могући нежељени ефекти или негативни исходи потенцијалне вакцине.
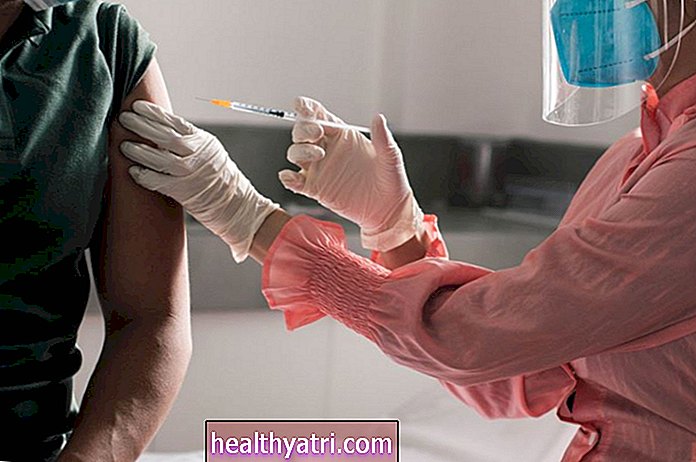
6. октобра, Управа за храну и лекове (ФДА) најавила је да ће захтевати од произвођача вакцина ЦОВИД-19 да деле два месеца података о безбедности пре него што одобри вакцину за употребу у широј јавности. Одлука ФДА долази тамо где постоји расте јавно неповерење у сигурност будуће ЦОВИД вакцине.
ЦОВИД-19 вакцине: Будите у току са доступним вакцинама, ко их може добити и колико су сигурне.
Нови захтеви ФДА
Према новим захтевима ФДА, мораће бити два месеца додатних података о здрављу добровољаца у клиничким испитивањима након што приме друге дозе вакцине. ФДА може одлучити да произвођачу вакцина додели одобрење за хитну употребу —Ознака која омогућава јавну употребу производа — ако су испуњени нови захтеви.
Схобха Сваминатхан, МД
Сигурност је кључна у срцу обезбеђивања да људи верују послу који радимо.
- др Схобха СваминатханФДА је у својим смерницама објаснила да жели да види податке из фазе 3 испитивања када су учесници завршили пуни режим вакцинације и два месеца након тога. ФДА верује да ће овај временски оквир пружити „адекватне информације за процену профила користи и ризика вакцине“.
Према смерницама, ФДА ће размотрити „нежељене догађаје; случајеве тешке болести ЦОВИД-19 међу испитаницима; и случајеве ЦОВИД-19 који се јављају током временског периода када су адаптивни (уместо урођени) и имунолошки одговори на вакцину. би био одговоран за заштитни ефекат “.
ФДА такође каже да треба да постоји „довољан број случајева озбиљног ЦОВИД-19 међу испитаницима“ како би се доказало да постоји мали ризик од људи који ће развити озбиљне компликације од вакцине.
Поред тога, ФДА очекује да произвођачи покажу податке који се односе на одређене синдроме - посебно на појачану респираторну болест повезану са вакцином (ЕРД) из вакцине. „Укупно пет или више тежих случајева ЦОВИД-19 у плацебо групи обично би било довољно да се процени да ли тешки случај ЦОВИД-19 који се дели између група вакцина и плацебо подржава повољан профил користи и ризика или обратно изазива забринутост. "
Тренутно постоји 11 вакцина у фази 3 (завршна фаза) клиничких испитивања, међутим, неколико испитивања која је спровело неколико главних фармацеутских компанија недавно је паузирано након што је барем један учесник студије развио озбиљну, необјашњиву болест.
Случај двомјесечног чекања
„Мислим да је сјајно што ФДА тражи да имамо два месеца сигурносних података“, стручњак за заразне болести Схобха Сваминатхан, др. Мед., Ванредни професор и главни истражитељ испитивања вакцине Модерна ЦОВИД-19 на Медицинској школи Рутгерс Нев Јерсеи Центар за клиничка истраживања, каже Веривелл. „Сигурност је пресудна у срцу обезбеђивања да људи верују послу који радимо.“
Сваминатхан објашњава да се најчешћи нежељени ефекти од вакцина јављају у року од два месеца. „Већина нежељених ефеката вакцине, попут грознице, умора и реакција на месту ињекције, јавља се током прве недеље, а сложенији се могу јавити током шест недеља. Зато су корисна најмање два месеца да би се открило шта се може догодити. “
Схобха Сваминатхан, МД
Не журите са закључцима о научном процесу. Пуно је дезинформација.
- др Схобха СваминатханСваминатхан каже да временски оквир „покушава да уравнотежи јавне потребе без угрожавања сигурности.“ Нада се да ће смернице ФДА помоћи у промени перцепције јавности о процесу развоја вакцине.
„У јавности постоји перцепција да се истраживање вакцина против ЦОВИД-19 убрзава пре рока, а неки људи су забринути да то долази по цену безбедносних мера, што заправо није тачно“, каже Сваминатхан. „ФДА утврдиће да ли су безбедносне информације које имају [од истраживача] одговарајуће. “
Све у свему, Сваминатхан позива људе да верују процесу. „Не журите са закључцима о научном процесу. Много је погрешних информација. “
Шта ово значи за вас
Захтев ФДА за двомјесечним подацима о праћењу након што људи приме ЦОВИД-19 вакцину треба да помогне да се осигура да се евентуални нежељени ефекти ухвате пре него што вакцина постане доступна широј јавности. Међутим, процес би на крају могао потрајати дуже.
Јавност би требало да верује да је поступак развоја и одобравања вакцине сигуран и да ФДА неће одобрити вакцину док не буде спремна и сигурна.














-and-alcohol.jpg)






